- GRAS (MÉTABOLISME DES ACIDES)
- GRAS (MÉTABOLISME DES ACIDES)Les acides gras représentent l’unité de base des diverses classes de lipides: phospholipides, lipides neutres, esters de stéroïdes, etc. Rarement présents dans la matière vivante sous forme libre, ils existent surtout sous forme combinée et leur rôle est essentiel dans le déroulement des processus vitaux. Dans le tissu adipeux, par suite de leur faible conductibilité thermique, ils participent à la protection des organismes vis-à-vis du milieu extérieur. Ils forment, en outre, une très importante substance de réserve, puisque leur dégradation libère une quantité d’énergie plus de deux fois supérieure à celle que fournirait un même poids de glucose. Enfin, sous forme combinée, ils prennent part dans les cellules à de nombreux processus métaboliques, tels que transport actif à travers les membranes, transport d’électrons de la chaîne respiratoire, intégration dans certains constituants fondamentaux du système nerveux... [cf. NEUROCHIMIE]. La dégradation des acides gras par oxydation conduit à la formation d’acétyl-coenzyme A, produit important du catabolisme glucidique [cf. GLUCIDES] et point de départ de la biosynthèse de ces mêmes acides suivant une voie différente de la première.StructureLes acides gras les plus répandus dans la nature contiennent seize ou dix-huit atomes de carbone, ces valeurs paires découlant de leur biosynthèse. Ils sont constitués d’un groupement carboxylique porté à l’extrémité d’une chaîne hydrocarbonée formée par un enchaînement linéaire de groupements méthylènes. Cette chaîne peut être saturée, insaturée, quelquefois ramifiée, ou comporter d’autres fonctions chimiques. Le tableau 1 résume les structures de quelques acides gras; les doubles liaisons, de configuration cis dans la plupart des chaînes insaturées (formules 1, 3, 4, 5 et 6), sont séparées les unes des autres par un méthylène lorsqu’il y en a plusieurs (formules 3 à 6).Dans les cellules, ces acides gras sont le plus souvent présents à l’état d’esters et entrent alors dans la constitution des substances plus complexes comme les glycérides, ou certains phospholipides. Plus rarement, ils peuvent exister à l’état d’amides comme dans les sphingolipides [cf. LIPIDES].DégradationAcides saturésL’étude du mécanisme de la dégradation des acides gras a débuté avec les travaux de F. Knoop (1904): des animaux, nourris avec des acides gras dans lesquels un cycle benzénique se substitue à un atome d’hydrogène sur le dernier carbone de la chaîne, excrètent dans l’urine (sous forme d’amides avec le glycocolle) des produits contenant un cycle benzénique et dont la nature varie selon que l’acide gras ingéré possède un nombre pair ou impair d’atomes de carbone (fig. 1). Ces résultats montrèrent que les acides gras se dégradent à partir du carboxyle par pertes successives de fragments de deux atomes de carbone. Il y a par conséquent oxydation du méthylène en position 廓 (c’est-à-dire du troisième atome de carbone à compter du carboxyle); c’est pour cette raison que ce processus fut appelé 廓-oxydation. Il fallut cependant attendre cinquante ans pour que le mécanisme en soit élucidé.On remarqua par la suite que l’énergie apportée par l’ATP était indispensable à l’oxydation des acides gras; on en conclut que l’acide gras devait être activé avant sa métabolisation. Vers 1945, une nouvelle coenzyme intervenant dans cette activation fut découverte. On lui donna le nom de coenzyme A ; on l’écrit CoA-SH pour mettre en évidence le groupement thiol par lequel agit ce composé; sa formule renferme, en effet, liée au nucléotide phosphorylé de l’adénine, une molécule de phosphopantéthéine dont le groupement terminal thiol est libre (cf. tableau 2).En 1951, F. Lynen montra que les acides gras se dégradent sous la forme de thioesters de coenzyme A, en libérant des fragments dicarbonés constitués d’acétyl-coenzyme A. Le mécanisme de la 廓-oxydation fut alors élucidé, les enzymes et composés intermédiaires isolés et identifiés. Le schéma, représenté à la figure 2 a, dans lequel l’acide palmitique est pris comme exemple, est appelé « hélice de Lynen »; chaque réaction est catalysée par une enzyme différente. L’oxydation complète d’un acide gras nécessite la répétition d’un cycle de quatre réactions consécutives à l’activation de l’acide palmitique par la coenzyme A, l’énergie nécessaire à cette activation étant fournie par l’hydrolyse d’une molécule d’ATP. La palmitoyl-coenzyme A (1) obtenue est d’abord oxydée en acide 見, 廓-insaturé (2), de configuration trans, grâce à une enzyme à flavine (FAD), puis hydratée en 廓-hydroxy-palmitoyl-coenzyme A (3) de configuration L (+). Une déshydrogénase à NAD+ oxyde le dérivé 廓-hydroxylé (3) en ester 廓-cétonique (4) qui, avec l’intervention conjuguée d’une nouvelle molécule de coenzyme A et de l’enzyme correspondante (thiolase), est scindé en une molécule d’acétyl-coenzyme A (5) (acétate actif) et une molécule d’une acyl-coenzyme A (6) contenant deux atomes de carbone de moins que l’acide de départ. Cet ester, dans une deuxième spire de l’hélice, va subir la même suite de quatre réactions que la palmitoyl-coenzyme A, libérant ainsi une nouvelle molécule d’acétyl-coenzyme A et l’ester de l’acide en C12. Ainsi, par pertes successives de deux atomes de carbone, l’acide palmitique est transformé en huit molécules d’acétyl-coenzyme A, après sept cycles.Cette dégradation n’a pas produit d’énergie; elle a, en fait, consommé une molécule d’ATP. La totalité de l’énergie libérée dans le catabolisme des acides gras est fournie, d’une part par l’oxydation des coenzymes réduites (FADH2 et NADH) par l’intermédiaire de la phosphorylation oxydative mitochondriale, d’autre part par la dégradation ultérieure de l’acétyl-coenzyme A dans le cycle de Krebs.L’oxydation des acides gras est ainsi directement couplée à la chaîne respiratoire de la cellule et au cycle de Krebs (fig. 6). La chaîne des transporteurs d’électrons de la phosphorylation oxydative productrice d’ATP se trouve placée sur les crêtes de la membrane mitochondriale interne, alors que les enzymes du cycle de Krebs et de la 廓-oxydation sont localisées à l’intérieur de la mitochondrie.Acides insaturésLes acides mono- et polyinsaturés sont dégradés par 廓-oxydation à partir du carboxyle jusqu’au voisinage de la première double liaison (fig. 3). Par exemple, l’acide oléique (1) (cis-octadécène-9 oïque) est catabolisé en ester 廓, 塚-insaturé cis-dodécène-3 oïque (2); ce dernier est transformé par une isomérase en trans-dodécène-2-oate (3), intermédiaire de la 廓-oxydation dans l’hélice de Lynen. La suite des réactions se poursuit alors jusqu’à dégradation totale par le mécanisme décrit à la figure 2 a. Pour les acides polyinsaturés, le processus est identique, avec une variante: l’acide 廓, 塚-insaturé cis obtenu est isomérisé en acide 見, 廓-insaturé trans, puis entre dans les cycles de l’hélice de Lynen; lorsque, par 廓-oxydation, on est conduit à un acide 見, 廓-insaturé cis, celui-ci est hydraté en D (face=F0019 漣) 廓-hydroxy-acide, puis isomérisé en L (+) 廓-hydroxy-acide, intermédiaire de la dégradation.Il existe divers autres systèmes de catabolisme des acides gras:– l’ 見-oxydation , qui dégrade une chaîne d’acide gras libre, atome de carbone par atome de carbone, avec formation de C2. Deux systèmes d’ 見-oxydation sont connus. L’un, spécifique des végétaux, fait intervenir une peroxydase. Le second, opératif chez les animaux, les végétaux et les organismes procaryotes, utilise l’oxygène moléculaire et conduit à la formation, comme intermédiaire, d’acides gras 見-hydroxylés.– l’ 諸-oxydation , qui conduit à la transformation du méthyle terminal en un carboxyle. Ce processus fait intervenir dans une première phase une hydroxylase à cytochrome P-450 (en présence de 2 et NADPH) transformant l’acide gras en 諸-hydroxy-acide, puis une déshydrogénase à NAD dans une seconde phase.Ces différents systèmes peuvent intervenir successivement pour dégrader un acide gras: lorsque la 廓-oxydation est bloquée par une fonction présente dans la chaîne de l’acide saturé (ramification en 廓 par exemple), l’oxydation en 見 ou en 諸 se produit, et, à partir des nouvelles fonctions acides ainsi créées, la chaîne peut être à nouveau dégradée par 廓-oxydation. Citons, en particulier, l’ 見-oxydation de l’acide phytanique (produit du métabolisme du phytol, alcool diterpénique contenu dans la chlorophylle) qui, étant un acide 廓-méthyl ramifié, ne peut pas être dégradé par 廓-oxydation. Une 見-oxydation transforme l’acide phytanique en acide nor-phytanique, acide 見-méthyl ramifié, dégradable par 廓-oxydation.BiosynthèseOn distingue la synthèse de novo des acides gras qui, à partir d’acétate, conduit à la synthèse d’acide gras en C16, accompagné d’un peu d’acides en C14 et C18, et l’élongation des acides gras, qui permet de synthétiser des acides à très longue chaîne à partir d’acide palmitique.Acides saturésLes réactions successives permettant de dégrader les acides gras selon le schéma de Lynen étant réversibles, on pouvait se demander si leur synthèse n’était que le schéma inverse de la 廓-oxydation. En fait le fonctionnement en sens inverse (avec intervention d’une réductase finale spécifique de la synthèse) n’intervient que dans l’élongation des acides gras (fig. 2 b).En 1957, à partir du cytoplasme de foie de pigeon, Wakil isolait un complexe enzymatique, séparable en deux fractions qui, réunies, permettent la synthèse de novo d’acides gras en l’absence de toute enzyme de 廓-oxydation. La première de ces fractions était une enzyme ayant la biotine comme coenzyme (acétyl-CoA-carboxylase); elle catalyse la transformation d’acétyl-CoA en malonyl-CoA par fixation de gaz carbonique (tabl. 1, réaction 1). La deuxième (acide-gras-synthétase) transformait l’acétate et le malonate en acides gras (principalement terme en C16), en présence de NADPH.En recherchant des intermédiaires de cette synthèse catalysée par une acide-gras-synthétase d’origine bactérienne, P. Roy Vagelos a observé que ces intermédiaires étaient liés à une protéine particulière, qu’il a isolée en 1963 et appelée ACP (du nom anglais acyl carrier protein ). L’ACP est une protéine de poids moléculaire voisin de 9 000 contenant une chaîne de pantéthéine-phosphate fixée sur l’hydroxyle d’un résidu de sérine de la partie polypeptidique (tabl. 2); cette chaîne provient de la coenzyme A.Elle est aujourd’hui connue sous le nom d’acide gras syntase ou synthétase.Un système dit ACP-dépendant a d’abord été décrit chez des organismes procaryotes tels que Escherichia coli . Deux trans-acylases catalysent le transfert des radicaux acétyl et malonyl de la coenzyme A à l’ACP, conduisant à la formation d’acétyl-ACP et de malonyl-ACP (fig. 2 b).Acétyl-ACP et malonyl-ACP se condensent, libérant une molécule de C2 et l’ACP, et fournissant une acéto-acétyl-ACP (1), qui est réduite en ester d’acide D (face=F0019 漣) 廓-hydroxybutyrique (2), puis déshydratée en trans-crotonyl-ACP (3). Cet ester 見, 廓-insaturé est alors réduit en butyryl-ACP (4). L’hydrogène nécessaire à ces deux réductions est apporté par NADPH. À ce stade, une boucle de l’hélice a été parcourue. La butyryl-ACP se condense avec une nouvelle molécule de malonyl-ACP, et la même suite de réactions répétées sept fois permet la synthèse de palmitoyl-ACP. Des transférases ou des hydrolases permettent alors de former la palmitoyl-coenzyme A ou l’acide palmitique, ou l’incorporent directement dans des lipides complexes. La stœchiométrie de la réaction globale conduisant à l’acide palmitique est:
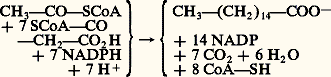 Tandis que, dans le système précédent, chaque réaction est catalysée par une enzyme distincte, isolable, les systèmes ACP-indépendants sont constitués par 2 ou même 1 seule chaîne polypeptidique portant non seulement toutes les activités enzymatiques, mais encore une chaîne de pantéthéine-phosphate (c’est-à-dire un ACP intégré).L’un des systèmes le mieux connu est celui de la levure (fig. 4). L’acide-gras-synthétase de levure a été isolée sous la forme d’un complexe protéique du type 見6 廓6, c’est-à-dire résultant de l’association de 6 chaînes 見 et 6 chaînes 廓. Les chaînes 見, P.M. 213 000, portent la chaîne pantéthéine-phosphate, une cystéine qui apporte un -SH «périphérique», et les activités 廓-céto-acyl-synthétase et 廓-céto-acyl-réductase. Les chaînes 廓, P.M. 203 000, portent les activités acétyl-transacylase, malonyl-transacylase, déshydratase et énoyl-réductase. Le fait que deux protéines seulement interviennent est confirmé par des études génétiques qui montrent que la synthèse de l’acide-gras-synthétase est codée par deux gènes seulement, fas 1 et fas 2.L’acide-gras-synthétase isolée de tissus animaux (en particulier du foie) se comporte comme un dimère (P.M. environ 500 000) formé de deux sous-unités identiques. Sur chaque chaîne polypeptidique sont donc localisées les six activités enzymatiques, la chaîne de pantéthéine-phosphate et le -SH périphérique (Wakil, 1981).La biosynthèse des acides gras a lieu dans le cytosol cellulaire; les mitochondries fournissent les groupements acétyle par l’intermédiaire du cycle pyruvate-oxaloacétate-citrate qui permet la traversée de leur membrane; une navette malate-pyruvate assure le transfert de pouvoir réducteur lié au NADP [cf. MITOCHONDRIES]. L’élongation des acides gras se produit dans la membrane de reticulum endoplastique des cellules eucaryotes.Acides insaturésAcides mono-insaturésLes acides mono-insaturés se forment principalement par deux voies:– La voie de synthèse utilisée par la plupart des organismes est la désaturation des acides saturés correspondants; ainsi, chez les animaux, la stéaroyl-coenzyme A (chez une Algue, c’est la stéaroyl-ACP) est désaturée en oléate par un système utilisant l’oxygène et le NADPH; cette désaturation est stéréospécifique, puisque deux atomes d’hydrogène de configuration D sont enlevés.– Chez certaines bactéries anaérobies, l’acide vaccénique (cis-octadécène-11-oïque) est formé en introduisant l’insaturation au cours de la synthèse par allongement de la chaîne; l’oxygène n’est pas utilisé pour créer cette double liaison: l’acide octanoïque est obtenu par condensations maloniques successives (sous forme d’esters d’ACP), selon la figure 2 b déjà décrite. L’octanoyl-ACP (1, fig. 5 a) condensé avec une unité malonique (2) est transformé en 廓-céto-ester (3), puis réduit en 廓-hydroxy-ester (4). La déshydratation peut fournir le trans-décène-2-oate (5); en ce cas, les acides saturés se synthétisent selon la voie habituelle.Cet ester peut, par ailleurs, être déshydraté en cis-décène-3-oate (6), (l’enzyme catalyse aussi l’interconversion de ces deux esters insaturés), puis subir l’allongement par unités malonates; on obtient alors l’acide insaturé en C18.Acides polyinsaturésToutes les espèces de micro-organismes, les plantes et les animaux synthétisent des acides gras polyinsaturés dont les doubles liaisons sont séparées par un seul méthylène (cependant, la plupart des bactéries semblent dépourvues d’acides gras polyinsaturés).Les animaux supérieurs ne peuvent pas synthétiser de tels acides à partir de précurseurs saturés ou mono-insaturés usuels, mais ils produisent des acides polyinsaturés en C20 ou C22 à partir de l’acide linoléique, qui est un acide gras indispensable. Les systèmes enzymatiques permettent à la fois l’allongement de la chaîne et la désaturation entre le carboxyle et la première insaturation (fig. 5 b).Les plantes, les levures et les algues vertes, au contraire, transforment l’acide oléique en acides polyinsaturés, mais désaturent entre la double liaison et le méthyle terminal de la chaîne (fig. 5 c).Enfin, d’autres micro-organismes peuvent synthétiser ces acides en utilisant indifféremment un processus ou l’autre.Les acides gras polyinsaturés, principalement l’acide arachidonique, peuvent être transformés dans les tissus animaux en substances biologiquement actives à des doses extrêmement faibles: prostaglandines, thromboxanes, prostacyclines, leukotriènes.Relations entre les métabolismesDégradation et synthèse des acides gras sont liées par la voie de l’acétyl-coenzyme A à la glycolyse, à la gluconéogenèse et au cycle de Krebs (fig. 6). Par l’intermédiaire des coenzymes d’oxydo-réduction, ces métabolismes interfèrent avec la phosphorylation oxydative (processus générateur d’ATP); il existe de nombreuses autres relations, notamment avec le métabolisme des aminoacides. Ces divers métabolismes sont de plus en plus en relation constante par le truchement des systèmes de régulation. Par exemple, l’enzyme permettant la carboxylation de l’acétyl-coenzyme A (et par conséquent la synthèse des acides gras) est activée par le citrate (métabolite du cycle de Krebs). Or, ce composé s’accumule dans la cellule lorsque celle-ci est pauvre en AMP, c’est-à-dire lorsqu’elle n’a pas besoin d’énergie. En ce cas, l’acétyl-CoA formé est transformé en acide gras qui est une forme de mise en réserve de l’énergie et la glycolyse est bloquée par inhibition de la phosphofructokinase, enzyme clef de celle-ci. Tous ces liens mettent en évidence l’unité métabolique de la cellule vivante, où les divers métabolismes sont dépendants, non seulement par l’intermédiaire de leurs substrats, mais aussi par la participation de ceux-ci aux phénomènes de régulation.
Tandis que, dans le système précédent, chaque réaction est catalysée par une enzyme distincte, isolable, les systèmes ACP-indépendants sont constitués par 2 ou même 1 seule chaîne polypeptidique portant non seulement toutes les activités enzymatiques, mais encore une chaîne de pantéthéine-phosphate (c’est-à-dire un ACP intégré).L’un des systèmes le mieux connu est celui de la levure (fig. 4). L’acide-gras-synthétase de levure a été isolée sous la forme d’un complexe protéique du type 見6 廓6, c’est-à-dire résultant de l’association de 6 chaînes 見 et 6 chaînes 廓. Les chaînes 見, P.M. 213 000, portent la chaîne pantéthéine-phosphate, une cystéine qui apporte un -SH «périphérique», et les activités 廓-céto-acyl-synthétase et 廓-céto-acyl-réductase. Les chaînes 廓, P.M. 203 000, portent les activités acétyl-transacylase, malonyl-transacylase, déshydratase et énoyl-réductase. Le fait que deux protéines seulement interviennent est confirmé par des études génétiques qui montrent que la synthèse de l’acide-gras-synthétase est codée par deux gènes seulement, fas 1 et fas 2.L’acide-gras-synthétase isolée de tissus animaux (en particulier du foie) se comporte comme un dimère (P.M. environ 500 000) formé de deux sous-unités identiques. Sur chaque chaîne polypeptidique sont donc localisées les six activités enzymatiques, la chaîne de pantéthéine-phosphate et le -SH périphérique (Wakil, 1981).La biosynthèse des acides gras a lieu dans le cytosol cellulaire; les mitochondries fournissent les groupements acétyle par l’intermédiaire du cycle pyruvate-oxaloacétate-citrate qui permet la traversée de leur membrane; une navette malate-pyruvate assure le transfert de pouvoir réducteur lié au NADP [cf. MITOCHONDRIES]. L’élongation des acides gras se produit dans la membrane de reticulum endoplastique des cellules eucaryotes.Acides insaturésAcides mono-insaturésLes acides mono-insaturés se forment principalement par deux voies:– La voie de synthèse utilisée par la plupart des organismes est la désaturation des acides saturés correspondants; ainsi, chez les animaux, la stéaroyl-coenzyme A (chez une Algue, c’est la stéaroyl-ACP) est désaturée en oléate par un système utilisant l’oxygène et le NADPH; cette désaturation est stéréospécifique, puisque deux atomes d’hydrogène de configuration D sont enlevés.– Chez certaines bactéries anaérobies, l’acide vaccénique (cis-octadécène-11-oïque) est formé en introduisant l’insaturation au cours de la synthèse par allongement de la chaîne; l’oxygène n’est pas utilisé pour créer cette double liaison: l’acide octanoïque est obtenu par condensations maloniques successives (sous forme d’esters d’ACP), selon la figure 2 b déjà décrite. L’octanoyl-ACP (1, fig. 5 a) condensé avec une unité malonique (2) est transformé en 廓-céto-ester (3), puis réduit en 廓-hydroxy-ester (4). La déshydratation peut fournir le trans-décène-2-oate (5); en ce cas, les acides saturés se synthétisent selon la voie habituelle.Cet ester peut, par ailleurs, être déshydraté en cis-décène-3-oate (6), (l’enzyme catalyse aussi l’interconversion de ces deux esters insaturés), puis subir l’allongement par unités malonates; on obtient alors l’acide insaturé en C18.Acides polyinsaturésToutes les espèces de micro-organismes, les plantes et les animaux synthétisent des acides gras polyinsaturés dont les doubles liaisons sont séparées par un seul méthylène (cependant, la plupart des bactéries semblent dépourvues d’acides gras polyinsaturés).Les animaux supérieurs ne peuvent pas synthétiser de tels acides à partir de précurseurs saturés ou mono-insaturés usuels, mais ils produisent des acides polyinsaturés en C20 ou C22 à partir de l’acide linoléique, qui est un acide gras indispensable. Les systèmes enzymatiques permettent à la fois l’allongement de la chaîne et la désaturation entre le carboxyle et la première insaturation (fig. 5 b).Les plantes, les levures et les algues vertes, au contraire, transforment l’acide oléique en acides polyinsaturés, mais désaturent entre la double liaison et le méthyle terminal de la chaîne (fig. 5 c).Enfin, d’autres micro-organismes peuvent synthétiser ces acides en utilisant indifféremment un processus ou l’autre.Les acides gras polyinsaturés, principalement l’acide arachidonique, peuvent être transformés dans les tissus animaux en substances biologiquement actives à des doses extrêmement faibles: prostaglandines, thromboxanes, prostacyclines, leukotriènes.Relations entre les métabolismesDégradation et synthèse des acides gras sont liées par la voie de l’acétyl-coenzyme A à la glycolyse, à la gluconéogenèse et au cycle de Krebs (fig. 6). Par l’intermédiaire des coenzymes d’oxydo-réduction, ces métabolismes interfèrent avec la phosphorylation oxydative (processus générateur d’ATP); il existe de nombreuses autres relations, notamment avec le métabolisme des aminoacides. Ces divers métabolismes sont de plus en plus en relation constante par le truchement des systèmes de régulation. Par exemple, l’enzyme permettant la carboxylation de l’acétyl-coenzyme A (et par conséquent la synthèse des acides gras) est activée par le citrate (métabolite du cycle de Krebs). Or, ce composé s’accumule dans la cellule lorsque celle-ci est pauvre en AMP, c’est-à-dire lorsqu’elle n’a pas besoin d’énergie. En ce cas, l’acétyl-CoA formé est transformé en acide gras qui est une forme de mise en réserve de l’énergie et la glycolyse est bloquée par inhibition de la phosphofructokinase, enzyme clef de celle-ci. Tous ces liens mettent en évidence l’unité métabolique de la cellule vivante, où les divers métabolismes sont dépendants, non seulement par l’intermédiaire de leurs substrats, mais aussi par la participation de ceux-ci aux phénomènes de régulation.
Encyclopédie Universelle. 2012.
